28/01/2018
Imagina que tienes un vaso de agua y le echas una cucharada de sal. La revuelves y, ¡magia!, la sal desaparece, o al menos no la ves. Lo que tienes ahora es una mezcla. Es una mezcla especial porque la sal se ha disuelto en el agua, creando lo que llamamos una solución de agua salada. Pero, ¿qué pasa si ahora quieres separar la sal del agua? ¿Cómo podrías recuperar el agua limpia y la sal por otro lado? No puedes simplemente colarla como si fuera pasta. Necesitas un truco de ciencia, y ese truco se llama destilación.
La destilación es un proceso muy útil que nos permite separar los componentes de una mezcla líquida, especialmente cuando uno de esos componentes se evapora más fácilmente que el otro. En nuestro caso, el agua se evapora mucho más fácil que la sal. La sal, de hecho, no se evapora nada a las temperaturas a las que hierve el agua. Esto es clave para la destilación.

Entendiendo la Mezcla de Agua y Sal
Antes de separar, entendamos qué es una mezcla. Cuando mezclas sal y agua, las pequeñas partículas de sal (iones) se dispersan y se rodean de las partículas de agua (moléculas). Están todas mezcladas juntas de forma uniforme. No es solo un montón de sal en el fondo del vaso (a menos que hayas puesto demasiada sal), sino que la sal está realmente *en* el agua, disuelta. Para separar esta mezcla y recuperar el agua, necesitamos hacer que el agua cambie de estado.
El agua puede estar en diferentes estados: como hielo (sólido), como agua líquida, o como vapor (gas). La destilación aprovecha el cambio de estado del agua de líquido a vapor y luego de vapor a líquido nuevamente.
El Proceso de Destilación: Paso a Paso
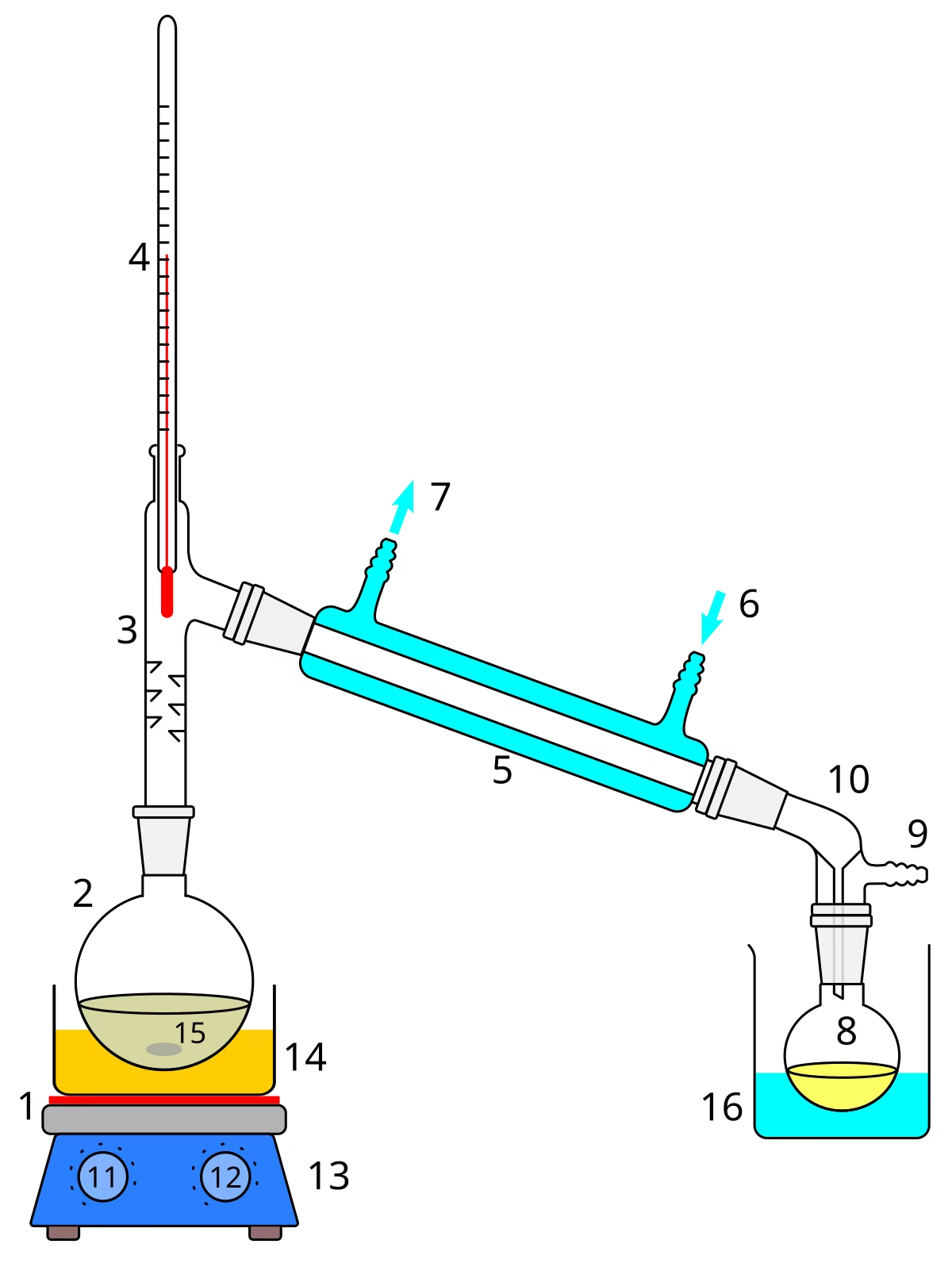
Para separar la sal del agua mediante destilación en un laboratorio, podríamos usar un equipo especial diseñado para esto. Piensa en ello como una especie de 'máquina de separación' para líquidos.
El proceso comienza colocando la solución de agua salada en un recipiente de vidrio que podemos calentar, como un matraz. Este matraz se coloca sobre una fuente de calor, como un mechero Bunsen.
Cuando calentamos la solución de agua salada, las partículas de agua en el líquido empiezan a moverse muy, muy rápido. Cuanto más calor añadimos, más energía tienen estas partículas y más rápido se mueven. Llega un punto, que para el agua pura es a 100 grados Celsius (el punto de ebullición), en el que estas partículas de agua tienen tanta energía que pueden escapar de la superficie del líquido y convertirse en vapor de agua, que es agua en estado gaseoso.
Es importante notar que, mientras el agua se convierte en vapor, la sal se queda atrás en el matraz. La sal tiene un punto de ebullición mucho, mucho más alto que el del agua, por lo que a la temperatura en la que el agua hierve, la sal sigue siendo un sólido disuelto o, si el agua se evapora por completo, se quedaría como un sólido en el fondo.
La Parte Clave: El Condensador
El vapor de agua que se forma sube y sale del matraz. Aquí es donde entra en juego otra pieza importante del equipo: un condensador. Un condensador es básicamente un tubo que está rodeado por otro tubo por donde circula agua fría constantemente.
Imagina un tubo hueco por el medio. El vapor de agua caliente viaja por este tubo central. Alrededor de este tubo central hay una especie de 'manga' o 'chaqueta' por la que hacemos pasar agua fría. Esta agua fría entra por la parte de abajo del condensador y sale por la parte de arriba. ¿Por qué por abajo y sale por arriba? Para asegurar que todo el espacio alrededor del tubo central se llene de agua fría y se mantenga lo más frío posible de manera eficiente.
Cuando el vapor de agua caliente, que se mueve muy rápido, entra en contacto con las paredes frías del tubo central del condensador, le ocurre lo contrario que cuando lo calentamos: pierde energía. Las partículas de vapor de agua, al enfriarse, se mueven más lento y empiezan a juntarse de nuevo. Este proceso se llama condensación, y es cuando el vapor de agua vuelve a convertirse en agua líquida.
Piensa en lo que pasa en el espejo del baño cuando te duchas con agua caliente: el vapor de agua caliente toca la superficie fría del espejo y se convierte en gotitas de agua. Eso es condensación.
Recogiendo el Agua Pura
El agua líquida formada por la condensación gotea lentamente por el tubo inclinado del condensador y cae en otro recipiente que hemos colocado al final, como un cilindro graduado o un vaso de precipitados. Este recipiente recoge el agua que ha sido separada de la sal.
Lo que recogemos en este recipiente es agua pura. Ya no contiene la sal que estaba disuelta en la mezcla original. En el matraz donde empezamos, si calentamos hasta que toda el agua se evapore, quedaría la sal sola en el fondo.
Así, hemos logrado separar la sal del agua: el agua se ha convertido en vapor y luego de nuevo en líquido puro, mientras que la sal se ha quedado en el recipiente original.
Resumen del Proceso
Podemos resumir el proceso de destilación simple así:
- Tenemos una mezcla (agua salada).
- Calentamos la mezcla.
- El agua se convierte en vapor de agua (evaporación). La sal se queda atrás.
- El vapor de agua viaja a un lugar frío (el condensador).
- El vapor de agua se enfría y vuelve a ser agua líquida (condensación).
- Recogemos el agua pura.
Es como si el agua hiciera un viaje: sale de la mezcla como vapor, se limpia en el camino (dejando la sal atrás) y vuelve a ser agua líquida y pura en otro lugar.
Comparando la Mezcla y los Resultados
Podemos ver las diferencias clave entre la mezcla inicial y las sustancias que obtenemos al final del proceso de destilación simple:
| Característica | Mezcla Inicial (Agua Salada) | Resultado (Agua Pura) | Resultado (Sal Restante) |
|---|---|---|---|
| Sabor | Salado | Sin sabor (neutro) | Salado (sólido) |
| Composición | Agua + Sal disuelta | Principalmente H₂O | Principalmente NaCl (Cloruro de Sodio) |
| Estado inicial | Líquido | Líquido (recogido) | Sólido (queda en el matraz) |
| Punto de Ebullición | Ligeramente más alto que el agua pura | 100°C (a nivel del mar) | Muy alto |
| Proceso de Obtención | Mezclando | Por condensación del vapor de agua | Queda en el matraz después de evaporar el agua |
Aplicaciones de la Destilación
Aunque hemos usado el ejemplo sencillo de separar agua y sal, la destilación es un proceso fundamental en muchas áreas. Por ejemplo, en la industria química, la destilación se utiliza para separar mezclas de líquidos que tienen diferentes puntos de ebullición. Un ejemplo muy importante de esto es la separación de los diferentes componentes del petróleo crudo.
El petróleo crudo que se extrae de la tierra es una mezcla compleja de muchos líquidos diferentes, como la gasolina, el diésel, el queroseno, etc. Cada uno de estos líquidos hierve a una temperatura diferente. Mediante un proceso de destilación más complejo (llamado destilación fraccionada), se calienta el petróleo crudo y los diferentes componentes se evaporan y condensan a distintas alturas en una torre, permitiendo separarlos. Así se obtienen los combustibles y otros productos que usamos a diario.
Preguntas Curiosas sobre la Destilación
- ¿Por qué la sal no se evapora con el agua?
- La sal (cloruro de sodio) es un compuesto iónico que tiene fuerzas de atracción muy fuertes entre sus partículas. Se necesita muchísima más energía (una temperatura mucho más alta que la del agua hirviendo) para romper estas uniones y que la sal pase a estado gaseoso. Por eso, a la temperatura de ebullición del agua, la sal se queda atrás en el recipiente.
- ¿El agua que se recoge es totalmente pura?
- Sí, en una destilación simple ideal, el vapor de agua que se condensa es agua pura (H₂O), libre de las sales disueltas y otras impurezas no volátiles (que no se evaporan fácilmente). Es uno de los métodos para obtener agua muy pura.
- ¿Se puede separar alcohol del agua usando destilación?
- Sí, de hecho, la destilación se usa mucho para separar líquidos con diferentes puntos de ebullición, como el alcohol y el agua. El alcohol (etanol) hierve a una temperatura más baja (aproximadamente 78°C) que el agua (100°C). Al calentar una mezcla de alcohol y agua, el alcohol se evapora más rápido y en mayor proporción que el agua, permitiendo obtener un vapor más rico en alcohol que luego se condensa.
- ¿Es este proceso igual que la desalinización del agua de mar?
- La desalinización del agua de mar para obtener agua potable a gran escala a menudo utiliza procesos basados en la evaporación y condensación, que son principios similares a la destilación. Sin embargo, las plantas desalinizadoras modernas a menudo usan técnicas más eficientes energéticamente, como la ósmosis inversa, además de la destilación u otros métodos térmicos.
- ¿Qué queda en el matraz al final?
- Si se evapora toda el agua, en el matraz inicial quedará la sal que estaba disuelta. Si solo se evapora una parte del agua, quedará una solución de agua salada más concentrada.
Como puedes ver, la destilación es un principio científico muy elegante y práctico. Nos enseña cómo los diferentes puntos de ebullición de las sustancias pueden ser usados para separarlas, transformando un mezcla en sus componentes puros mediante cambios de estado como la evaporación y la condensación. Es un recordatorio de que la ciencia nos ofrece herramientas ingeniosas para entender y modificar el mundo que nos rodea.
Si quieres conocer otros artículos parecidos a ¿Cómo Separar Agua y Sal? La Destilación puedes visitar la categoría Ciencia.
